Wie wir im letzten Kapitel gesehen haben, ist das Universum einige Sekunden nach dem Urknall mit einem sehr dichten und heißen Plasma aus Protonen, Neutronen, Elektronen, Photonen, Neutrinos und Antineutrinos sowie den geheimnisvollen Teilchen der dunklen Materie angefüllt. Die Zahl der Photonen ist sehr viel größer als die Zahl der Protonen, Neutronen und Elektronen. Das Plasma ist gleichsam von gleißender Röntgen- und Gammastrahlung durchdrungen.
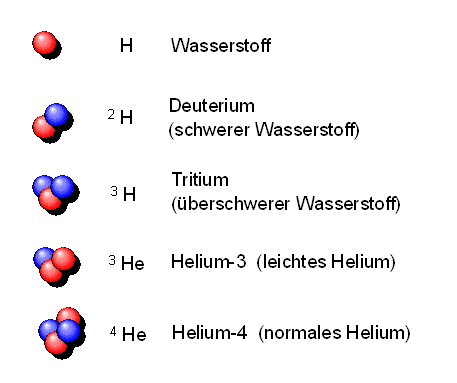
Wenn die Temperatur nach etwa 3 Minuten den Bereich von einer Milliarde Kelvin ( 109 K ) erreicht, verbinden sich zunehmend mehr Protonen und Neutronen zu sogenanntem Deuteriumkernen, ohne dass diese gleich wieder zerstört werden. Mit der Bildung von Deuteriumkernen ist der Weg nun frei, dass sich weitere Protonen bzw. Neutronen anlagern können. Lagert sich ein Neutron an einen Deuteriumkern an, so entsteht ein Tritiumkern (auch überschwerer Wasserstoff genannt und mit 3H abgekürzt). Lagert sich dagegen ein Proton an, so entsteht der leichte Heliumisotopkern 3He . In beiden Fällen lagert sich bevorzugt ein weiteres Proton oder Neutron so an, dass ein normaler Heliumkern 4He aus 2 Protonen und 2 Neutronen entsteht. Dieser Heliumkern ist sehr stabil, viel stabiler als der Deuteriumkern zuvor.

Nun ist man jedoch in einer Sackgasse: Es gibt keine stabilen Atomkerne mit 5 Nukleonen.

Wie sieht es mit anderen Möglichkeiten zur Bildung schwererer Atomkerne aus? Könnten nicht zwei Helium-3-Kerne zusammen einen Berillium-6-Kern bilden? Doch auch hier haben wir Pech: Berillium-6 ( 6Be ) ist nicht stabil. Ähnlich ist es mit zwei Helium-4-Kernen: Berillium-8 ist auch nicht stabil (es gibt überhaupt keinen stabilen Atomkern mit 8 Nukleonen, analog zu 5 Nukleonen).
Eine wichtige Möglichkeit wäre noch die 3-Körper-Reaktion, bei der aus drei Helium-4-Kernen ein Kohlenstoff-12-Kern ( 12C ) entsteht. Dafür ist jedoch die Helium-Teilchendichte bereits zu gering, denn es müssen fast gleichzeitig drei Helium-4-Kerne zusammentreffen. Erst viel später wird diese Reaktion, die man auch als Heliumbrennen oder Drei-Alpha-Prozess bezeichnet, im Inneren von Sternen stattfinden können. Fast alle schweren Atomkerne sind aus Kohlenstoff entstanden, der zuvor über diesen Prozess in Sternen gebildet wurde.
Schwere Atomkerne wie beispielsweise Kohlenstoffkerne oder Eisenkerne entstehen also kurz nach dem Urknall praktisch überhaupt nicht und können erst später im Inneren von Sternen gebildet und freigesetzt werden, besonders dann, wenn große Sterne am Ende ihres Lebens als Supernova explodieren.
Insgesamt nehmen Temperatur und Dichte während der Bildung neuer Atomkerne nach dem Urknall ständig schnell ab, so dass nur ein relativ kleines Zeitfenster zur Bildung größerer Atomkerne bleibt. Die Zahl der noch freien Neutronen nimmt weiter aufgrund der Bildung von Helium und aufgrund des Neutronzerfalls ab, und Protonen können sich schließlich bei niedrigeren Temperaturen nicht mehr an andere Atomkerne anlagern, da sowohl Atomkerne als auch Protonen elektrisch positiv geladen sind und sich daher abstoßen. Nach etwa 20 bis 30 Minuten kommt daher die Bildung neuer Atomkerne vollständig zum erliegen, während die wenigen noch freien Neutronen weiter zerfallen. Bilder zur zeitlichen Entwicklung der primordialen Nukleosynthese (so nennt man die Bildung neuer Atomkerne nach dem Urknall) findet man im Internet beispielsweise unter http://www.astro.ucla.edu/~wright/BBNS.html sowie http://www.fas.org/irp/imint/docs/rst/Sect20/A1.html oder auch http://www.astro.virginia.edu/class/whittle/astr124/matter/BBNS_vs_t.html (oder einfach mal im Internet Bilder zu "Big Bang nucleosynthesis" suchen).
Letztlich werden praktisch alle Neutronen zur Bildung von normalen stabilen Helium-4-Kernen ( 4He ) verbraucht. Lediglich einige wenige Deuteriumkerne ( 2H ), Helium-3-Kerne ( 3He ) und Tritiumkerne ( 3H ) bleiben übrig. Bei den schweren Elementen Berillium-7, Lithium-6 und Lithium-7 gibt es nur sehr geringe Anteile.
Als die Bildung von Deuteriumkernen einsetzt, liegt das Zahlenverhältnis von Protonen zu Neutronen bei etwa 7 zu 1. Da praktisch alle Neutronen in Heliumkernen enden, folgt daraus:
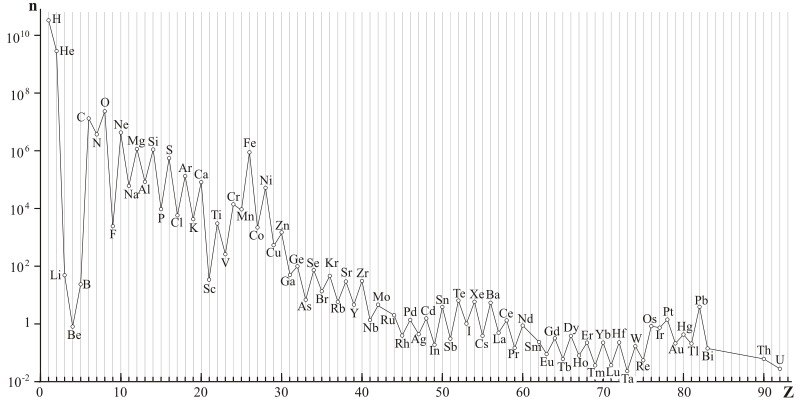
Der Gewichtsanteil der Heliumatome am Gewicht aller Atome sollte etwa 25 Prozent betragen. Die anderen 75 Gewichtsprozent sind fast ausschließlich Wasserstoff! Das sollte auch heute noch im Wesentlichen so sein, und tatsächlich findet man dieses Massenverhältnis, wenn man die durchschnittliche Verteilung der chemischen Elemente im heutigen Universum betrachtet. Nur ein Atom von 1000 ist nicht Wasserstoff oder Helium.
Literatur zu dem Thema:
last modified on 17 February 2012